Ο αμερικανικός Οργανισμός Τροφίμων και Φαρμάκων (FDA) έδωσε ταχεία έγκριση στο Wegovy της εταιρείας Novo Nordisk για τη θεραπεία της μη αλκοολικής λιπώδους νόσου του ήπατος σε ενήλικες με μέτρια έως προχωρημένη ίνωση, αλλά χωρίς κίρρωση.
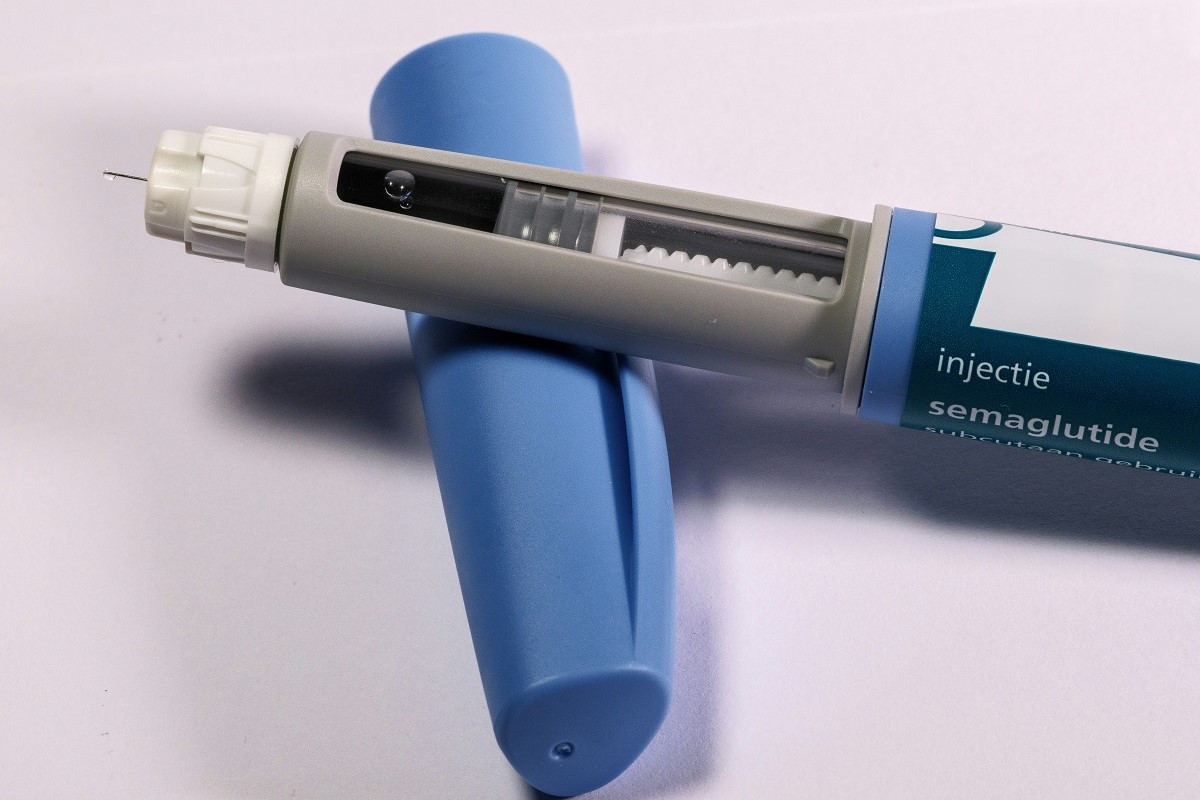
Το φάρμακο, που χορηγείται μία φορά την εβδομάδα σε διαβητικούς ασθενείς ως υποδόρια ένεση σεμαγλουτίδης 2,4 mg, συνδυάζεται με διατροφή μειωμένων θερμίδων και περισσότερη σωματική δραστηριότητα.
Υπολογίζεται ότι 1 στους 3 υπέρβαρους ή παχύσαρκους ανθρώπους παγκοσμίως έχει και μη αλκοολική λιπώδη νόσο του ήπατος.
Πόσο αποτελεσματικό ήταν το Wegovy
Η απόφαση βασίστηκε στα αποτελέσματα του πρώτου μέρους της μελέτης ESSENCE φάσης 3. Εκεί, το Wegovy έδειξε σημαντική βελτίωση στην ίνωση του ήπατος χωρίς επιδείνωση της στεατοηπατίτιδας, αλλά και υποχώρησή της, χωρίς επιδείνωση της ίνωσης, σε σύγκριση με το εικονικό φάρμακο, στην εβδομάδα 72. Τα δεδομένα αυτά δημοσιεύθηκαν τον Απρίλιο στο New England Journal of Medicine.
Στη μελέτη συμμετείχαν 800 άτομα: 534 έλαβαν Wegovy και 266 εικονικό φάρμακο, πάντα σε συνδυασμό με αλλαγές στον τρόπο ζωής. Η μέση ηλικία ήταν 56 έτη και ο μέσος ΔΜΣ 34. Οι περισσότεροι συμμετέχοντες ήταν λευκοί (67,5%) και γυναίκες (57,1%), ενώ πάνω από τους μισούς (55,9%) είχαν σακχαρώδη διαβήτη τύπου 2. Συνολικά, 250 άτομα (31,3%) είχαν ίνωση σταδίου ΙΙ και 550 (68,8%) ίνωση σταδίου ΙΙΙ. Οι ασθενείς λάμβαναν σταθερές θεραπείες για λιπίδια, σακχαρώδη διαβήτη και απώλεια βάρους.
Στην εβδομάδα 72, το πρώτο βασικό αποτέλεσμα έδειξε ότι το 63% των ασθενών που έλαβαν Wegovy πέτυχαν υποχώρηση της στεατοηπατίτιδας χωρίς επιδείνωση της ίνωσης, έναντι 34% στην ομάδα του εικονικού φαρμάκου.
Το δεύτερο βασικό αποτέλεσμα έδειξε ότι το 37% όσων έλαβαν Wegovy εμφάνισαν βελτίωση της ίνωσης χωρίς επιδείνωση της στεατοηπατίτιδας, έναντι 22% στην ομάδα ελέγχου.
Σε ένα τρίτο καταληκτικό σημείο, το 33% των ασθενών που έλαβαν Wegovy παρουσίασαν τόσο υποχώρηση της στεατοηπατίτιδας όσο και βελτίωση της ίνωσης, έναντι 16% στην ομάδα του εικονικού φαρμάκου.
Επιπλέον, το 83,5% των ασθενών στην ομάδα της σεμαγλουτίδης διατήρησαν τη δόση-στόχο των 2,4 mg μέχρι την εβδομάδα 72.
Το Wegovy έχει επίσης ένδειξη για μείωση του κινδύνου σοβαρών καρδιαγγειακών επεισοδίων σε ενήλικες με γνωστή καρδιοπάθεια και παχυσαρκία ή υπερβάλλον βάρος. Χορηγείται επίσης σε ενήλικες και παιδιά άνω των 12 ετών με παχυσαρκία, καθώς και σε ενήλικες με υπερβάλλον βάρος που έχουν προβλήματα υγείας σχετιζόμενα με το βάρος, ώστε να χάσουν κιλά και να διατηρήσουν την απώλεια.
Wegovy: Σχέδια για αγωγή με τη μορφή χαπιού
Τον Φεβρουάριο του 2025 η Novo Nordisk κατέθεσε αίτηση για έγκριση στην Ευρωπαϊκή Ένωση, ενώ τον Μάιο υπέβαλε αντίστοιχη αίτηση στην Ιαπωνία. Τον ίδιο μήνα, ο FDA αποδέχθηκε αίτηση για σεμαγλουτίδη από το στόμα 25 mg.
Η δεύτερη φάση της μελέτης ESSENCE αναμένεται να ολοκληρωθεί το 2029 και να δείξει αν το Wegovy μειώνει τον κίνδυνο σοβαρών επιπλοκών από το ήπαρ, σε ασθενείς με μη αλκοολική λιπώδη νόσο του ήπατος και ίνωση F2 ή F3, στην εβδομάδα 240.
Παρότι η εταιρεία διαθέτει την τεχνολογία για χάπια σεμαγλουτίδης, διευκρίνισε ότι η κυκλοφορία τους στις ΗΠΑ για την παχυσαρκία θα εξαρτηθεί από τον προγραμματισμό του χαρτοφυλακίου και τη δυνατότητα παραγωγής. Η σεμαγλουτίδη από το στόμα σε δόση 50 mg δεν έχει ακόμη κατατεθεί σε ρυθμιστικές αρχές.
Όπως σημειώνει η εταιρεία, «η από του στόματος μορφή απαιτεί μεγαλύτερη ποσότητα δραστικής ουσίας (API). Εφόσον η διαθέσιμη ποσότητα είναι περιορισμένη, η ενέσιμη μορφή μάς δίνει τη δυνατότητα να καλύψουμε περισσότερους ασθενείς». Αυτή την περίοδο η Novo Nordisk επεκτείνει τις γραμμές παραγωγής σε παγκόσμιο επίπεδο, τόσο για τα ενέσιμα όσο και για τα χάπια, ώστε να καλύψει τη ζήτηση. Όμως, όπως υπογραμμίζει, «η διαδικασία χρειάζεται χρόνο για την κατασκευή, την εγκατάσταση, την πιστοποίηση και την πλήρη λειτουργία των νέων μονάδων».